 contact us
contact us
2026/04/10
利統股份有限公司 技術部保健品配方組 楊宗翰 博士、高念楚
帕金森氏症(Parkinson's Disease, PD)常被描述為一場發生在大腦深處、不為人知的「慢速火災」。從第一個神經元悄悄受損,到患者感受到手顫、步態僵硬,往往已歷經十年以上的無聲侵蝕 。這場火災的核心,是一個只有豌豆大小卻主掌全身動作協調的腦區-黑質(Substantia Nigra)。
當黑質神經元開始凋亡,多巴胺的供應鏈斷裂,人體的動作指揮中樞便逐漸失效 。科學界近年來愈來愈確信:氧化壓力(Oxidative Stress)與 神經發炎(Neuroinflammation)是這場火災中最關鍵的兩根柴薪。
根據世界衛生組織資訊,2019年全球已有超過850萬名患者,20年間盛行率增加了一倍 。而在台灣,65歲以上老年人盛行率約1%~2%,80歲以上更可達4% 。隨著台灣於2025年邁入「超高齡社會」,帕金森氏症已成為不容忽視的國民健康議題 。根據全球流行病學數據,帕金森氏症是繼阿茲海默症之後,全球第二大神經退化性疾病,隨著人口高齡化加速,預測至 2050 年,患病人數將突破 1,200 萬 1。
值得警惕的是,當患者出現典型運動症狀(如靜止性震顫、運動遲緩)而被確診時,黑質中的多巴胺神經元往往已喪失約 50% 至 70% 2 。這意味著臨床診斷的那一刻,大腦已獨自抵抗了漫長的退化歷程 。
⚠大腦的十年求救訊號—這些早期警訊,你注意到了嗎?
•嗅覺異常:無原因地對氣味變得遲鈍或失去嗅覺(可早於運動症狀 4–6 年)
•睡眠障礙:夜間手腳亂動、大聲說夢話(快速動眼期行為異常,RBD)
•慢性便秘:腸道神經叢是 Alpha-synuclein 最早堆積的地方之㇐
•情緒低落或憂鬱傾向:多巴胺系統受損連帶影響情緒調控迴路
•輕微記憶力或專注力下滑:非正常老化的「大腦霧感(Brain Fog)」
若上述症狀持續出現,建議及早就診神經科進行評估,並重視抗氧化與神經保護的日常介入。
帕金森氏症的病理核心可以視為一場在密閉空間中失控蔓延的火災 :
•α-突觸核蛋白 (α-synuclein) 堆積:這是越積越高、隨時引燃的「蛋白質垃圾堆」。它會破壞粒線體功能,是造成多巴胺神經元流失的重要病理因子3。
•氧化壓力 (Oxidative Stress):黑質先天對氧化壓力極其敏感,多巴胺代謝產生的自由基就像「火星」,不斷轟擊脆弱的神經元4。
•神經發炎:小膠質細胞原本是「免疫消防隊」,但在持續刺激下會轉變為「M1 促發炎型」,從消防員變身為「縱火犯」,加速神經凋亡5。
正當醫學界持續追尋能「修飾疾病進程」的解方,兩種天然來源的功能性成分 " 咪唑二肽與咖啡莓果中的活性因子 " 正以其深厚的科學佐證,在帕金森氏症的預防與輔助支持領域嶄露頭角。
咖啡被認為是具有預防帕金森氏症的潛力的素材,雖然日常飲用咖啡已被證實與降低帕金森氏症風險相關,但對於追求精準預防且不希望攝取過多咖啡因的族群來說,咖啡莓果提供了更進階的保護。研究顯示,咖啡莓果不僅含有綠原酸能調節細胞凋亡路徑,更是科學界認可的 BDNF 營養刺激劑,能針對帕金森氏症常見的認知功能下滑提供關鍵支援。
有研究顯示,帕金森氏症患者的血清中腦源性神經營養因子 (Brain-derived neurotrophic factor, BDNF) 濃度會顯著低於健康人,這可能是帕金森氏症會併發認知障礙的因素之一6。咖啡莓果萃取物是一種BDNF的營養刺激劑7,已在人體試驗上被證實可增加血液中的的BDNF濃度8,於預防及緩解帕金森氏症的症狀具有不錯的潛力。此外,咖啡莓果中也富含綠原酸 (Chlorogenic acid, CGA),綠原酸被發現可穿過血腦障壁,對於缺血性的大腦組織可發揮神經保護作用9,並可透過調控Akt與Erk1/2 訊號路徑抑制 ROS (Reactive oxygen species) 的產生來預防帕金森氏症的神經元凋亡10,且經綠原酸預處理的PC12細胞對於α-突觸核蛋白 (α-synuclein) 產生的神經毒性具有保護作用11,值得一提的是α-突觸核蛋白是一種位於神經元突觸前末端的蛋白質,帕金森氏症患者神經中的α-突觸核蛋白會出現大量累積錯誤的堆疊,導致製造多巴胺的神經元的傷害與流失,是造成帕金森氏症重要的病理因子,因此在此機制下,富含綠原酸的咖啡莓果亦是有助於預防帕金森氏症的潛力素材。
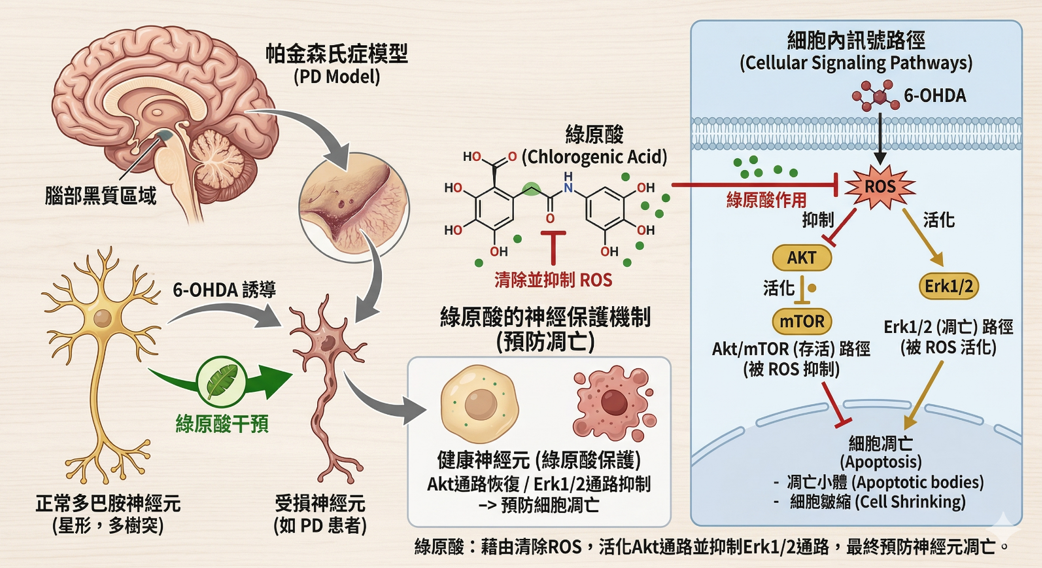 Figure : 綠原酸的神經保護作用:可透過調節 Akt與Erk1/2 訊號路徑來預防帕金森氏症的神經元凋亡 (參考並修改自He et al., 2024) 11。
Figure : 綠原酸的神經保護作用:可透過調節 Akt與Erk1/2 訊號路徑來預防帕金森氏症的神經元凋亡 (參考並修改自He et al., 2024) 11。
咪唑二肽是指肌肽 (Carnosine) 及甲肌肽 (Anserine) 這兩種的胜肽成分,主要存在於雞胸肉、魚肉等食物中。有相關文獻發現帕金森氏症患者的大腦皮質中肌肽及甲肌肽的含量偏低12,且帕金森氏症患者腦脊髓液中的甲肌肽含量也顯著低於健康人13。然而,Zhao等人 (2017) 使用大鼠腦內皮細胞中建立的Salsolinol誘導帕金森氏症細胞模型,發現觀察給予肌肽具有保護神經的作用14,主要機制可能來自肌肽降低了ROS (Reactive oxygen species)的產生,並提升了抗氧化酶的活性。依上述結果來看,帕金森氏症患者的症狀之所以隨時間增加而惡化的因素之一,可能與帕金森氏症患者腦部皮質會缺乏抗氧化相關的胜肽有關,因此補充具有抗氧化能力的咪唑二肽,有助於減少神經元的氧化損傷15。
此外,關於帕金森氏症的關鍵病理因子α-突觸核蛋白,在動物試驗的層面發現以鼻內給藥 (Intranasal) 的方式補充肌肽 (Carnosine),可讓帕金森氏症小鼠模顯著降低嗅覺上皮細胞的α-突觸核蛋白累積,並顯著改善運動障礙16;後續有學者也使用了類似的動物模型深入分析肌肽對後帕金森氏症小鼠腦部的影響17,試驗結果發現,以鼻內給藥的方式補充肌肽能能明顯減輕帕金森氏症模型小鼠的運動障礙,並發現能顯著減少帕金森氏症小鼠大腦黑質緻密部 (Substantia nigra pars compacta, SNpc) 中α-突觸核蛋白的累積。雖然上述試驗並非使用傳統食用方式補充肌肽,用鼻內給藥的優勢在於可避開血腦障壁進入大腦,增加吸收速度並加強效果,因此仍能在動物試驗上證明補充肌肽確實具有改善帕金森氏症的潛力。
目前的病理研究尚未能完全斷定帕金森氏症的單一成因,但已知年齡老化、基因變異、環境毒素(如農藥、殺蟲劑等)及頭部外傷等,皆是誘發大腦黑質細胞退化的危險因子 。儘管來源不同,這些因子最終都匯聚成同一個毀滅性結果:神經元受損壞死導致多巴胺缺乏,引發後續的失能危機 。
面對這場「慢速火災」,預防的核心在於攔截氧化損傷與清除毒性蛋白 。近年科研實證,咖啡莓果與咪唑二肽能發揮協同作用,不僅有助於減少氧化壓力對神經元的傷害,更能降低病理標誌 α-突觸核蛋白的累積,守護珍貴的多巴胺神經元 。透過日常適量補充這些具備神經保護潛力的素材,我們能從多維度建立防護網,在症狀顯現前,提早為大腦爭取更多健康的空間 。
1. GBD 2016 Parkinson's Disease Collaborators. (2018). Global, regional, and national burden of Parkinson's disease, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. The Lancet Neurology, 17(11), 939–953.
2. Poewe, W., Seppi, K., Tanner, C. M., et al. (2017). Parkinson disease. Nature Reviews Disease Primers, 3, 17013.
3. Hirsch, E. C., & Hunot, S. (2009). Neuroinflammation in Parkinson's disease: a target for neuroprotection? The Lancet Neurology, 8(4), 382–397.
4. Meiser, J., Weindl, D., & Hiller, K. (2013). Complexity of dopamine metabolism. Cell Communication and Signaling, 11, 34.
5. Lull, M. E., & Block, M. L. (2010). Microglial activation and chronic neurodegeneration. Neurotherapeutics, 7(4), 354–365.
6.Wang, Y., Liu, H., Zhang, B. S., Soares, J. C., & Zhang, X. Y. (2016). Low BDNF is associated with cognitive impairments in patients with Parkinson’s disease. Parkinsonism & related disorders, 29, 66-71.
7. Cotter, J., Fawkes, N., & Shah, N. (2022). Coffee fruit extract–a nutritional stimulator of endogenous BDNF. Nutritional Neuroscience, 25(9), 2008-2010.
8. Reyes-Izquierdo, T., Nemzer, B., Shu, C., Huynh, L., Argumedo, R., Keller, R., & Pietrzkowski, Z. (2013). Modulatory effect of coffee fruit extract on plasma levels of brain-derived neurotrophic factor in healthy subjects. British Journal of Nutrition, 110(3), 420-425.
9. Lee, K., Lee, J. S., Jang, H. J., Kim, S. M., Chang, M. S., Park, S. H., ... & Bu, Y. (2012). Chlorogenic acid ameliorates brain damage and edema by inhibiting matrix metalloproteinase-2 and 9 in a rat model of focal cerebral ischemia. European journal of pharmacology, 689(1-3), 89-95.
10. He, S., Chen, Y., Wang, H., Li, S., Wei, Y., Zhang, H., ... & Zhang, R. (2024). Neuroprotective effects of chlorogenic acid: Modulation of Akt/Erk1/2 signaling to prevent neuronal apoptosis in Parkinson's disease. Free Radical Biology and Medicine, 222, 275-287.
11. Teraoka, M., Nakaso, K., Kusumoto, C., Katano, S., Tajima, N., Yamashita, A., ... & Matsura, T. (2012). Cytoprotective effect of chlorogenic acid against α-synuclein-related toxicity in catecholaminergic PC12 cells. Journal of clinical biochemistry and nutrition, 51(2), 122-127.
12. Kalecký, K., & Bottiglieri, T. (2023). Targeted metabolomic analysis in Parkinson’s disease brain frontal cortex and putamen with relation to cognitive impairment. npj Parkinson's Disease, 9(1), 84.
13. Öhman, A., & Forsgren, L. (2015). NMR metabonomics of cerebrospinal fluid distinguishes between Parkinson’s disease and controls. Neuroscience letters, 594, 36-39.
14. Zhao, J., Shi, L., & Zhang, L. R. (2017). Neuroprotective effect of carnosine against salsolinol-induced Parkinson's disease. Experimental and therapeutic medicine, 14(1), 664-670.
15. Solana-Manrique, C., Sanz, F. J., Martínez-Carrión, G., & Paricio, N. (2022). Antioxidant and neuroprotective effects of carnosine: therapeutic implications in neurodegenerative diseases. Antioxidants, 11(5), 848.
16. Bermúdez, M. L., Seroogy, K. B., & Genter, M. B. (2019). Evaluation of carnosine intervention in the Thy1-aSyn mouse model of Parkinson's disease. Neuroscience, 411, 270-278.
17. Brown, J. M., Baker, L. S., Seroogy, K. B., & Genter, M. B. (2021). Intranasal carnosine mitigates α-synuclein pathology and motor dysfunction in the Thy1-aSyn mouse model of Parkinson’s disease. ACS chemical neuroscience, 12(13), 2347-2359.